彫朎懱撪僇儖僔僂儉偺尭彮偵埶懚偟偨嬝暘壔惂屼婡峔
Tweet幏昅幰忣曬
幏昅幰丗拞惣宑巕丄怷搰怣桾
幏昅幰強懏丗崙棫尋媶奐敪朄恖丂棟壔妛尋媶強丂彫椦帀幙惗暔妛尋媶幒
尨挊榑暥丗Transient Ca2+ depletion from the endoplasmic reticulum is critical for skeletal myoblast differentiation. (The FASEB Journal 29:2137-2149, 2015)
峏怴擔丗2015擭7寧22擔
奣梫
儅僂僗崪奿嬝偺嵟廔暘壔夁掱偵偍偄偰丄彫朎懱僗僩儗僗偑堦夁揑偵惗偠丄偙傟偑暘壔偺恑峴偵昁恵偱偁傞偙偲傪巹偨偪偼埲慜曬崘偟偨丅偟偐偟丄暘壔偲偄偆惗棟揑忬嫷壓偵偍偄偰壗偑彫朎懱僗僩儗僗傪堷偒婲偙偟偰偄傞偺偐偼晄柧偱偁偭偨丅杮尋媶偱巹偨偪偼彫朎懱撪僇儖僔僂儉屚妷偵傛偭偰桿摫偝傟傞摿庩側彫朎懱枌峔憿傪尒弌偟丄偙傟傪巜昗偲偡傞偙偲偱嬝暘壔恑峴偵偲偭偰昁恵偱偁傞彫朎懱僗僩儗僗尮偑彫朎懱撪僇儖僔僂儉屚妷偱偁傞偙偲傪撍偒巭傔偨丅
偼偠傔偵
崪奿嬝偺嵟廔暘壔夁掱偼丄嬝夎嵶朎偑懡悢梈崌偟偰懡妀偺嬝娗嵶朎偵側傝丄峏偵梈崌傪孞傝曉偟側偑傜嬝慇堐嵶朎傊偲惉弉偟偰偄偔夁掱乮埲壓丄偙傟傪嬝暘壔夁掱偲屇傇乯偱偁傞丅嬝暘壔夁掱偱堦晹偺嬝夎嵶朎偼傾億僩乕僔僗傪婲偙偡丅偙偺傾億僩乕僔僗偑彫朎懱僗僩儗僗偲屇偽傟傞嵶朎僗僩儗僗偵傛偭偰堷偒婲偙偝傟傞偙偲丄彫朎懱僗僩儗僗偼嬝暘壔弶婜偵堦夁揑偵惗偠傞偙偲丄峏偵偼惗偒巆偭偨嵶朎偺暘壔偵偍偄偰傕彫朎懱僗僩儗僗僔僌僫儖偑昁梫偱偁傞偙偲傪巹偨偪偼柧傜偐偵偟偨乮侾乯丅
嵶朎撪彫婍姱偺堦偮偱偁傞彫朎懱偺栶妱偼懡婒偵傢偨傞丅慹柺彫朎懱偱崌惉偝傟偨枌僞儞僷僋幙丄暘斿僞儞僷僋幙偼偦偺撪峯偱棫懱峔憿宍惉丄摐嵔廋忺偑峴傢傟丄妸柺彫朎懱偼栻暔戙幱丄帀幙崌惉摍偺応偵側偭偰偄傞丅傑偨彫朎懱偼嵶朎偺庡梫側僇儖僔僂儉挋憼偺応偱偁傝丄嵶朎撪奜偺條乆側巋寖偵墳偠偰僇儖僔僂儉曻弌傪夘偟偰僇儖僔僂儉寢崌僞儞僷僋幙傪惂屼偟偰偄傞乮俀乯丅彫朎懱僗僩儗僗偼彫朎懱撪偵儈僗僼僅乕儖僨傿儞僌偟偨僞儞僷僋幙偑拁愊偟偨忬懺偲掕媊偝傟丄懡検偺僞儞僷僋幙崌惉丄堚揱巕曄堎傗僂僀儖僗姶愼丄僌儖僐乕僗婹夓丄彫朎懱撪僇儖僔僂儉掅壓摍偺條乆側梫場偵傛偭偰堷偒婲偙偝傟傞乮俁乯丅彫朎懱僗僩儗僗偼堦斒揑偵偼昦揑側忬懺偱偁傝丄嵶朎偵偲偭偰桳奞側傕偺偱偁傞丅偙傟偑惓忢側嬝暘壔夁掱偱偳偺傛偆偵惗偠偰偄傞偺偐丄偦偺庤偑偐傝傪摼傞偨傔偵巹偨偪偼彫朎懱枌峔憿偵拝栚偟偰夝愅傪峴偭偨丅
嬝暘壔夁掱偱彫朎懱枌桼棃偺媴忬峔憿偑堦夁揑偵弌尰偡傞
嬝暘壔偵敽偭偰嬝夎嵶朎偑嬝娗丄嬝慇堐嵶朎傊偲曄壔偡傞偲摨帪偵丄嵶朎撪偱偼彫朎懱偑嬝廂弅偺嵺偺僇儖僔僂儉曻弌偵揔偟偨宍懺丄婡擻傪帩偮嬝彫朎懱傊偲曄壔偡傞乮係乯丅巹偨偪偼偙偺嬝暘壔偵敽偭偨彫朎懱偺曄壔偑彫朎懱僗僩儗僗偺敪惗偲壗傜偐偺娭楢偑偁傞偺偱偼側偄偐偲峫偊丄嬝暘壔帪偺彫朎懱偺宍懺曄壔傪宱帪揑偵娤嶡偟偨丅
In vitro暘壔宯偱彫朎懱傪娤嶡偡傞偨傔丄儅僂僗嬝夎嵶朎姅C2C12嵶朎傪憹怋攟抧偐傜暘壔攟抧偵堏偡偙偲偵傛傝嬝暘壔桿摫傪峴偭偨丅暘壔攟抧偵堏偝傟偨嬝夎嵶朎偼栺嶰擔偐傜堦廡娫偐偗偰懡妀偺嬝娗嵶朎傊暘壔偡傞丅偙偺娫偺彫朎懱傪丄彫朎懱枌摿堎揑側寀岝昗幆帋栻偱偁傞ER Tracker傪梡偄偰壜帇壔偟偨丅
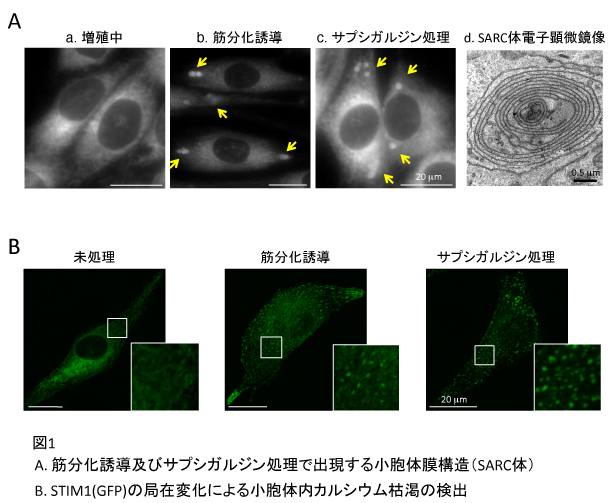
偦偺寢壥丄嵶朎梈崌偑婲偙傞捈慜偺嵶朎偵偍偄偰ER Tracker偱昗幆偝傟傞媴忬峔憿傪敪尒偟偨乮恾1A(a),(b)乯丅偙偺媴忬峔憿偼暘壔偺恑峴偲嫟偵彫偝偔側傝丄嵶朎梈崌偑恑傫偱妀悢偑10妀掱搙偵側傞崰偵偼傎傏徚幐偡傞丅椶帡偟偨媴忬峔憿偼儅僂僗戀巈偺嬝敪惗帪偵偍偄偰傕娤嶡偝傟偨丅巹偨偪偼埲慜偺尋媶偱丄嬝慇堐偑嶌傜傟偮偮偁傞戀楊13.5擔儅僂僗泱偺崪奿嬝慻怐偵偍偄偰彫朎懱僗僩儗僗偑敪惗偡傞偙偲傪曬崘偟偰偄傞乮侾乯丅偙偺慻怐拞偱丄摿偵嬝僞儞僷僋幙偺敪尰偑婲偙傝巒傔傞慜偺丄傛傝枹暘壔側嵶朎偵偍偄偰ER Tracker梲惈偺媴忬峔憿偑懡悢娤嶡偝傟偨丅攟梴宯偱偺宱夁偲摨條偵暘壔偑恑傫偩嵶朎拞偱偼媴忬峔憿偼徚幐偟偰偄偨丅
彫朎懱枌桼棃偺媴忬峔憿偼彫朎懱撪僇儖僔僂儉屚妷偵傛傝桿摫偝傟傞
媴忬峔憿偑彫朎懱僗僩儗僗埶懚揑偵宍惉偝傟傞偐傪専摙偡傞偨傔丄嶌梡婡彉偺堎側傞彫朎懱僗僩儗僗桿摫栻嵻傪梡偄偰C2C12嵶朎傪張棟偟偨屻丄彫朎懱傪娤嶡偟偨丅梡偄偨栻嵻偼丄彫朎懱僇儖僔僂儉ATP傾乕僛乮彫朎懱撪偵僇儖僔僂儉傪庢崬傓栶妱傪扴偆乯傪慾奞偡傞僒僾僔僈儖僕儞媦傃僔僋儘僺傾僝儞巁丄彫朎懱撪摐嵔廋忺慾奞嵻偱偁傞僣僯僇儅僀僔儞丄彫朎懱乕僑儖僕懱娫桝憲慾奞嵻偱偁傞僽儗僼僃儖僨傿儞A偱偁傞丅
彫朎懱僗僩儗僗墳摎偵傛偭偰敪尰偑桿摫偝傟傞揮幨場巕CCAAT/enhancer-binding protein homologous protein (CHOP)偑偳偺栻嵻張棟偱傕専弌偝傟偨偺偵懳偟丄嬝暘壔帪偲摨條偺媴忬峔憿偼彫朎懱撪僇儖僔僂儉擹搙掅壓傪堷偒婲偙偡僒僾僔僈儖僕儞媦傃僔僋儘僺傾僝儞巁偱張棟偟偨応崌偵偍偄偰摿堎揑偵宍惉偝傟偨乮恾1A(c)乯丅偙偺寢壥偼ER Tracker偱壜帇壔偝傟傞摿庩側媴忬峔憿偼彫朎懱僗僩儗僗偵昁偢敽偭偰惗偠傞偺偱偼側偔丄彫朎懱撪僇儖僔僂儉屚妷偵埶懚偟偨彫朎懱僗僩儗僗偵傛偭偰摿堎揑偵惗偠傞峔憿偱偁傞偙偲傪帵嵈偟偰偄傞丅僒僾僔僈儖僕儞偱張棟偟偨C2C12嵶朎偺彫朎懱傪宱帪揑偵娤嶡偟偨寢壥丄張棟屻栺2帪娫偱惗偠偨媴忬峔憿偼8帪娫崰偐傜彫偝偔側傝丄36帪娫屻偵偼傎傏徚幐偟偨丅偙偺傛偆偵偄偭偨傫宍惉偝傟偨媴忬峔憿偑傗偑偰彫偝偔側偭偰徚幐偡傞宱夁偼嬝暘壔夁掱偱尒傜傟偨尰徾偲嫟捠偟偰偄傞丅
C2C12嵶朎偺嬝暘壔桿摫帪媦傃彫朎懱撪僇儖僔僂儉屚妷桿摫帪偵惗偠傞彫朎懱枌桼棃偺媴忬峔憿傪摟夁揹巕尠旝嬀偵傛傝徻偟偔娤嶡偟偨寢壥丄彫朎懱枌偑壗憌偵傕愊傒廳側偭偨摨怱媴峔憿傪偲傞偙偲偑柧傜偐偲側偭偨乮恾侾A(d)乯丅偙偺峔憿偼旕忢偵摿挜揑偱丄嵟奜憌偺枌偼儕儃僜乕儉偺晅拝偟偨慹柺彫朎懱偲宷偑偭偰偄傞偑丄摨怱媴峔憿撪晹偺枌偼妸柺忬偱偁傝丄彫朎懱撪峯偼旕忢偵嫹偔側偭偰偄傞偐丄傕偟偔偼枌娫娫寗偑傎偲傫偳尒傜傟側偔側偭偰偄偨丅偙傟傜偺摿挜偼嬝暘壔桿摫帪偲彫朎懱撪僇儖僔僂儉屚妷桿摫帪偱嫟捠偟偰偄偨丅
嬝暘壔夁掱偱堦夁揑偵惗偠傞彫朎懱撪僇儖僔僂儉屚妷偑SARC懱宍惉偲彫朎懱僗僩儗僗傪堷偒婲偙偡
嬝暘壔桿摫偵傛偭偰惗偠傞彫朎懱枌桼棃媴忬峔憿偑彫朎懱撪僇儖僔僂儉屚妷偵傛偭偰桿摫偝傟傞壜擻惈偑嫮偔帵嵈偝傟偨偙偲偐傜丄嬝暘壔帪偵偍偗傞彫朎懱撪僇儖僔僂儉擹搙曄壔傪彫朎懱撪僇儖僔僂儉僙儞僒乕偱偁傞stromal interaction molecule 1 (STIM1)僞儞僷僋幙偺嬊嵼僀儊乕僕儞僌偵傛偭偰壜帇壔偡傞偙偲傪帋傒偨丅彫朎懱枌娧捠僞儞僷僋幙偱偁傞STIM1偼彫朎懱僇儖僔僂儉擹搙偑崅偔曐偨傟偰偄傞応崌偵偼彫朎懱枌忋偵嬒堦偵暘晍偟偰偄傞偑丄彫朎懱撪僇儖僔僂儉屚妷帪偵偼彫朎懱枌忋偱懡検懱傪宍惉偟丄彫朎懱偲嵶朎枌偑嬤愙偟偰偄傞椞堟偵嬊嵼偡傞偨傔尠旝嬀壓偱偼僪僢僩僷僞乕儞偲偟偰娤嶡偝傟傞乮俆乯丅
寀岝僞儞僷僋幙GFP傪梈崌偟偨STIM1僞儞僷僋幙傪C2C12嵶朎撪偱敪尰偝偣丄暘壔攟抧偵堏偟偰宱帪揑娤嶡傪峴偭偨寢壥丄嬝暘壔桿摫屻24帪娫慜屻偵堦夁揑偵僪僢僩僷僞乕儞偑娤嶡偝傟偨乮恾1B乯丅彫朎懱僗僩儗僗墳摎僞儞僷僋幙CHOP偺敪尰偼暘壔桿摫屻24帪娫偐傜48帪娫偱婲偙傞偙偲偐傜丄STIM1偵傛偭偰壜帇壔偝傟偨彫朎懱撪僇儖僔僂儉屚妷偼彫朎懱僗僩儗僗敪惗偺捈慜偵惗偠偰偄傞偲尵偊傞丅偙傟偼嬝暘壔偵敽偭偰惗偠傞彫朎懱僗僩儗僗偺尨場偑彫朎懱撪僇儖僔僂儉屚妷偱偁傞偙偲傪巟帩偡傞丅巹偨偪偼彫朎懱撪僇儖僔僂儉屚妷帪偵惗偠傞彫朎懱枌桼棃媴忬峔憿傪丄彫朎懱撪僇儖僔僂儉屚妷偵傛傞僗僩儗僗偑堷偒婲偙偡墳摎(stress-activated response to ER Ca2+ depletion)偲偄偆堄枴偲丄嬝擏傪昞偡塸岅偺愙摢帿sarc偵偐偗偰SARC 懱偲柤晅偗偨乮恾侾A乯丅
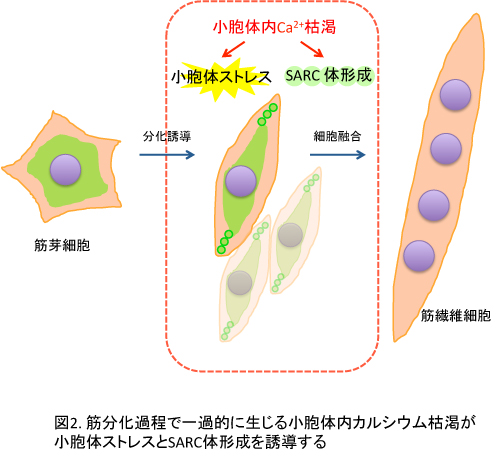
SARC懱偑彫朎懱撪僇儖僔僂儉屚妷偵傛偭偰桿摫偝傟傞峔憿偱偁傞偙偲傪慾奞嵻傪梡偄偨幚尡偵傛傝専徹偟偨丅C2C12嵶朎傪僒僾僔僈儖僕儞偱張棟偡傞偲摨帪偵丄彫朎懱偐傜偺僇儖僔僂儉曻弌傪扴偆庡梫側僇儖僔僂儉僠儍僱儖偱偁傞僀僲僔僩乕儖3儕儞巁乮IP3乯庴梕懱媦傃嬝宍惉偲偲傕偵敪尰偑忋徃偡傞僇儖僔僂儉僠儍僱儖偱偁傞儕傾僲僕儞庴梕懱傪慾奞偡傞偲SARC懱宍惉偼傎傏姰慡偵梷惂偝傟偨丅偙偺忦審壓偱偼彫朎懱撪僇儖僔僂儉偺弌擖傝偑摨帪偵巭傔傜傟丄彫朎懱撪僇儖僔僂儉擹搙偑崅偔曐偨傟偰偄傞偲峫偊傜傟傞丅C2C12嵶朎傪暘壔桿摫忦審偵偍偒丄摨帪偵IP3庴梕懱偲儕傾僲僕儞庴梕懱傪慾奞偡傞偲SARC懱宍惉丄彫朎懱僗僩儗僗墳摎丄嬝暘壔偺慡偰偑梷惂偝傟偨丅偙傟偼彫朎懱撪僇儖僔僂儉屚妷偑彫朎懱僗僩儗僗傪偼偠傔偲偡傞偙傟傜慡偰偺尰徾偺忋棳偵偁傞偙偲傪嫮偔帵嵈偟偰偄傞乮恾俀乯丅
偍傢傝偵
杮尋媶偵傛偭偰丄崪奿嬝偺宍惉夁掱偱惗偠傞彫朎懱僗僩儗僗偑彫朎懱撪僇儖僔僂儉偺屚妷偵傛偭偰惗偠偰偄傞偙偲偑嫮偔帵嵈偝傟偨丅彫朎懱僗僩儗僗偑嬝暘壔偵偲偭偰廳梫偱偁傞偙偲偐傜丄彫朎懱偺僇儖僔僂儉屚妷偼暘壔夁掱偵僾儘僌儔儉偝傟偨尰徾偱偁傞偲峫偊傜傟傞丅僾儘僌儔儉偝傟偨彫朎懱撪僇儖僔僂儉屚妷偑偳偺傛偆偵偟偰惗偠傞偺偐丄SARC懱偼偳偺傛偆側儊僇僯僘儉偱宍惉偝傟丄偳偺傛偆側婡擻傪帩偮偺偐摍丄怴偨側撲偑惗傑傟偨丅偙偺尋媶偺敪揥偑嬝敪惗偺惂屼婡峔偵偮偄偰偺棟夝傪怺傔丄峏偵偼榁壔傗昦婥丄夦変摍偵傛傞嬝擏偺悐偊偵懳偡傞帯椕朄奐敪偺堦彆偲側傞偙偲傪巹偨偪偼婅偭偰偄傞丅
嶲峫暥專
1. Nakanishi, K. et al. J. Cell Biol. 169, 555-560. (2005).
丂2. Bravo, R. et al. Int. Rev. Cell Mol. Biol. 301, 215-290 (2013).
丂3. Schroder, M. . Cell. Mol. Life Sci. 65, 862-894. (2008).
丂4. Al-Qusairi, L. and Laporte, J. Muscle 1:26. DOI:10.1186/2044-5040-1-26 (2011).
丂5. Wu, M. M. et al. J. Cell Biol. 174, 803-813. (2006).