執筆者自身による研究論文レビュー
Tweet執筆者:長谷川英一、七田崇、吉村昭彦
タイトル:IL-23-independent induction of IL-17 from γδT cells and innate lymphoid cells promotes experimental intraocular neovascularization.
更新日:2013年3月30日
原著論文:IL-23-independent induction of IL-17 from γδT cells and innate lymphoid cells promotes experimental intraocular neovascularization. The Journal of Immunology 190:1778-87, 2013.
執筆者所属:慶應大学医学部 微生物学・免疫学教室
概要
後天的失明原因の上位を占める加齢黄斑変性は脈絡膜血管新生を本態とする疾患である。今回我々はマウスの脈絡膜血管新生モデルを使って、炎症性サイトカインInterleukin(IL)-17が脈絡膜血管新生を促進することを明らかにした。また眼内におけるIL-17の産生細胞はTh17ではなくγδT細胞とInnate Lymphoid Cells(ILC)であり、これらの細胞はIL-23非依存的にIL-17を産生し得ることを示した。
***
はじめに
加齢黄斑変性(Age-related macular degeneration: AMD)は欧米の後天的失明原因の第1位であり、近年我が国においても高齢化に伴い患者数が増えている疾患である。AMDには滲出型と萎縮型があり、滲出型の主病態は脈絡膜血管新生(Choroidal neovascularization: CNV)である。CNVは網膜中心部の黄斑に生じやすく、容易に網膜下出血や滲出性変化を引き起こし黄斑機能低下による視力低下に繋がる。CNVの発生は網脈絡膜の加齢による構造変化に起因する限局的な慢性炎症がその原因と考えられており、その刺激により産生された血管内皮細胞増殖因子(Vascular endothelial growth factor: VEGF)を始めとする炎症性サイトカインがCNV形成に重要な役割を果たしていることが示唆されている。
近年、加齢黄斑変性の患者の血清中でIL-17量が上昇していることが報告された[1]。IL-17は主要な炎症性サイトカインで自己免疫疾患や炎症性疾患の発症において重要であり、関節リウマチや腫瘍においては血管新生作用を示すことが報告されている。本研究ではIL-17のCNV形成における役割を実験的レーザーCNVモデルを用いて検討した。
実験的レーザーCNVモデル
マウス脈絡膜にレーザー光凝固を行うことで炎症を励起し脈絡膜から血管新生を誘導することが出来る。レーザー照射後7日目にフルオレセイン標識デキストランを心腔内投与・潅流を行った後、眼球を摘出し脈絡膜フラットマウントを作成し病理組織学的に新生血管の形成を評価した[2]。
IL-17のCNV形成促進作用
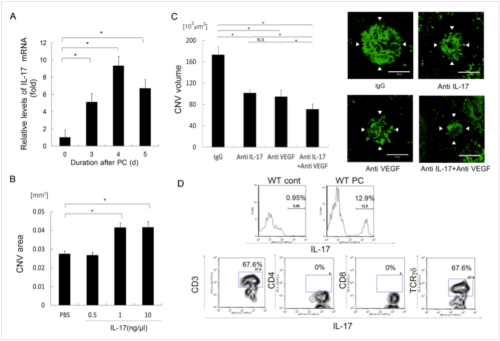
レーザー照射でCNV形成を誘導したマウスの眼内において、IL-17はレーザー照射後4日目で核酸レベルでの発現が最も上昇していた(図1A)。リコンビナントIL-17をレーザー照射直後眼内に投与するとCNV形成促進を認めた(図1B)。一方、レーザー照射直後にIL-17中和抗体を眼内に投与すると抗VEGF抗体と同等のCNV形成抑制効果が見られた(図1C)。またIL-17欠損マウスにおいてもレーザーによるCNV形成が有意に抑制されており、これらの結果によりIL-17が脈絡膜新生血管を促進することが示された。このIL-17の血管新生促進作用はVEGF非依存的であり、血管内皮細胞に直接働いていると考えられる。
眼内におけるIL-17産生細胞の同定
続いて眼内におけるIL-17産生細胞を同定するべくFACS解析を行った。IL-17の主要な産生細胞としてTh17細胞が知られているが、このモデルにおいてはTh17細胞ではなくγδT細胞が主要なIL-17産生細胞であることが分かった(図1D)。免疫染色にて障害された脈絡膜部位にγδT細胞が浸潤していることが確認された。除去抗体の投与によりγδT細胞を除去したマウスやTCTRδT欠損マウスにCNVを誘導するとIL-17発現量・CNV形成が抑制された。 近年、自然免疫に関与する新規の細胞群としてInnate Lymphoid Cells (ILC)が同定され、腸管ではIL-17を産生するILCも発見されている[3]。FACS解析の結果、眼内においてもγδT細胞の他にCD3-Thy1+のILCがIL-17を産生していることが示唆された。
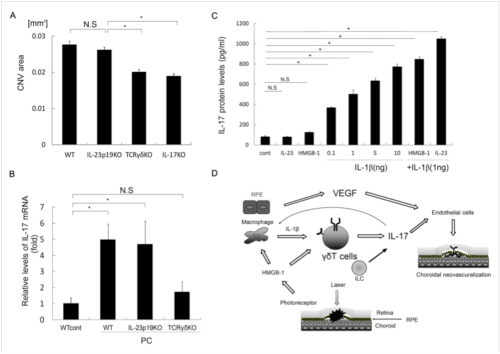
γδT細胞とInnate Lymphoid Cells(ILC)のIL-23非依存的IL-17産生機構
これらIL-17産生細胞のIL-17産生にはIL−1βとIL-23の両サイトカイン刺激が必須である[4]とされているが、レーザー照射されたIL-23p19欠損マウスの眼内においてもIL-17の発現上昇が見られCNV形成もWild typeマウスと同等である(図2A,B)ことから、眼内IL-17産生細胞はIL-23非依存的にIL-17を産生する機構が存在することが考えられた。 一方でIn vitroにおいてγδT細胞はIL−1β単独刺激のみ(IL-23刺激非存在下)でもIL-17を産生すること(図2C)、またIL-1 receptor antagonist 投与ではレーザー照射後の眼内IL-17発現量・CNV形成が共に抑制されることから、IL-1βはIL-17産生に重要な役割を果たしていることが示唆された。さらにIn vitroの実験でIL-1βとダメージ関連分子(DAMPs)の一つである核内蛋白質HMGB(High Mobility Group Box)-1との共刺激でγδT細胞からのIL-17産生がさらに上昇する(図2C)ことが分かった。眼内でのHMGB-1の発現はレーザー照射後上昇し、免疫染色でHMGB-1は障害された網膜色素上皮細胞や視細胞において発現が見られた。また抗HMGB-1抗体投与でIL-17発現量・CNV形成が抑制された。これらの結果より眼内のγδT細胞ではIL-17産生にIL-23刺激は必須ではなく、IL−1βやHMGB-1の刺激でIL-17を産生し得ることが示された(図2D)。
まとめ
本研究では炎症性サイトカインIL-17の脈絡膜血管新生促進作用とその産生機構について明らかにした。 抗IL-17抗体は現在臨床応用されている抗VEGF抗体と同等の血管新生抑制効果を示したことから、加齢黄斑変性の新たな治療のターゲットと成り得ると思われる。さらに今回の結果は加齢黄斑変性の他、糖尿病網膜症や網膜静脈分枝閉塞症等の眼内新生血管を引き起こす疾患の治療にも新たな可能性をもたらすものであると考える。
***
参考文献
1. Liu B et al., (2011) J Transl Med 9: 1-12.
2. Krzystolik MG et al., (2002) Arch Opthalamol 120: 338-346.
3. Buonocore S et al., (2010) Nature 464: 1371-1375.
4. Sutton CE et al., (2009) Immunity 31: 331-341.

