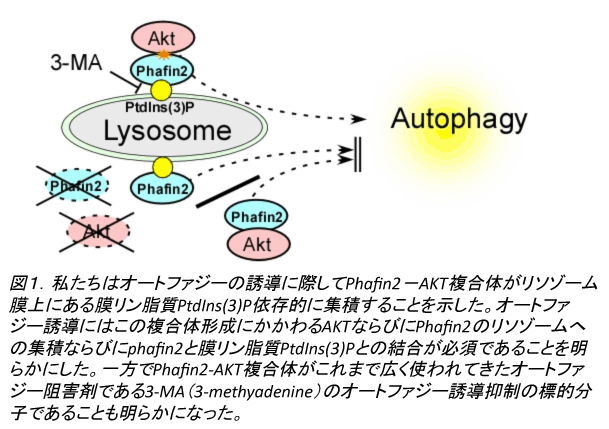
儕僜僝乕儉偵偍偗傞俙俲俿怴婯寢崌場巕Phafin2偵傛傞僆乕僩僼傽僕乕惂屼偺暘巕婡峔偺夝柧
Tweet幏昅幰忣曬
幏昅幰丗栰岥徆岾
幏昅幰強懏丗杒奀摴戝妛丂堚揱巕昦惂屼尋媶強丂娻惗暔暘栰丂嫵庼
尨挊榑暥丗Lysosomal Interaction of Akt with Phafin2: A Critical Step in the Induction of Autophagy. PLoS ONE 9:e79795, 2014.
峏怴擔丗2014擭2寧7擔
奣梫
僙儕儞僗儗僆僯儞僉僫乕僛AKT偼僆乕僩僼傽僕乕偺惂屼傊偺娭梌偑悇應偝傟偰偄傞偑丄 偦偺惂屼偺徻嵶偼晄柧偱偁偭偨丅巹偨偪偼AKT怴婯寢崌場巕偲偟偰儕僜僝乕儉抈敀Phafin2傪摨掕偟偨丅奺庬僆乕僩僼傽僕乕偺桿摫偵嵺偟偰Phafin2亅AKT暋崌懱偑儕僜僝乕儉枌忋偵偁傞枌儕儞帀幙PtdIns(3)P埶懚揑偵廤愊偡傞丅僆乕僩僼傽僕乕桿摫偵偼AKT側傜傃偵Phafin2偺儕僜僝乕儉傊偺廤愊偑昁恵偱偁傞丅
偼偠傔偵
歁擕摦暔嵶朎偺僙儕儞僗儗僆僯儞僉僫乕僛AKT乮Protein Kinase B乯偼丄嵶朎撪偵偍偗傞嵶朎巰乮傾億僩乕僔僗乯傗嵶朎惗懚惂屼偵偍偄偰嬌傔偰廳梫側摥偒傪偡傞嵶朎撪僔僌僫儖揱払場巕偱偁傞丅AKT僔僌僫儖揱払宯偼枌儕儞帀幙偺儕儞巁壔傪夘偟偰妶惈壔偝傟嵶朎巰乮傾億僩乕僔僗乯惂屼偺梫偺暘巕偲偟偰丄嵶朎巰丄嵶朎憹怋丄嵶朎廃婜丄抈敀崌惉丄寣娗怴惗丄摐戙幱側偳懡嵤側嵶朎斀墳傪惂屼偟偰偍傝丄偦偺惂屼婡峔偺攋抅偼條乆側僸僩偺幘昦偺尨場偲側傞偙偲偑抦傜傟偰偄傞丅AKT偼嵶朎奜偐傜偺巋寖偵傛傝class I 俹俬俁俲偵傛傞嶻暔偱偁傞枌儕儞帀幙俹俬(3,4,5)俹俁埶懚揑偵嵶朎枌傊堏峴偟丄AKT偺PH僪儊僀儞偵偙偺枌儕儞帀幙[PI乮3丆4丆5乯P3]偑寢崌偟丄PDK1丂(Phosphoinositide Dependent Kinase侾)偺摥偒偵傛傝僗儗僆僯儞308巆婎偑妶惈壔偝傟丄丂mTORC2暋崌懱偵傛偭偰僙儕儞473巆婎偑妶惈壔偝傟傞丅妶惈壔偝傟偨AKT偼FKHR丄BAD丄GSK3側偳條乆側嵶朎撪婎幙傪儕儞巁壔偟丄嵶朎巰傗嵶朎憹怋傪惂屼偡傞偙偲偑抦傜傟偰偄傞[1,2]丅
堦曽偱惗懱嵶朎偵偍偗傞惗棟婡擻偺峆忢惈偼嵶朎偺峔惉惉暘偱偁傞僞儞僷僋幙偺崌惉偲暘夝偺僶儔儞僗偵傛偭偰曐偨傟偰偄傞偲峫偊傜傟傞丅偙偺嵶朎撪偵偍偗傞庡偨傞僞儞僷僋幙暘夝宯偼丄儐價僉僠儞丒僾儘僥傾僜乕儉宯偵戙昞偝傟傞慖戰揑僞儞僷僋幙暘夝偲丄僆乕僩僼傽僕乕丒儕僜僜乕儉宯僞儞僷僋暘夝宯偵戙昞偝傟傞旕慖戰揑暘夝偲偵戝暿偝傟傞丅
僆乕僩僼傽僕乕偼嵶朎偑帩偭偰偄傞丄帺怘乮偠偟傚偔乯偲傕屇偽傟傞嵶朎撪偺僞儞僷僋幙傪暘夝偡傞偨傔偺巇慻傒偺堦偮偲峫偊傜傟丄峀媊偵偼儕僜僜乕儉偵偍偗傞嵶朎幙惉暘偺暘夝偺憤徧偱偁傞丅嬤擭丄歁擕摦暔偵偍偗傞僆乕僩僼傽僕乕偵娭梌偡傞堚揱巕孮(Atgs)偑師乆偲摨掕偝傟丄歁擕摦暔偵偍偗傞僆乕僩僼傽僕乕偺傕偮惗棟揑側堄媊側傜傃偵暘巕儗儀儖偱偺惂屼婡峔偑柧傜偐偵側偭偰偒偨[3]丅摿偵丄in vivo偵偍偗傞夝愅偵傛傝歁擕摦暔偵偍偗傞僆乕僩僼傽僕乕偺傕偮惗棟揑偝傜偵偼姶愼徢丄埆惈庮釃傪偼偠傔條乆側僸僩幘昦偺攚宨場巕偲偟偰偺栶妱偑拲栚偝傟偰偄傞丅
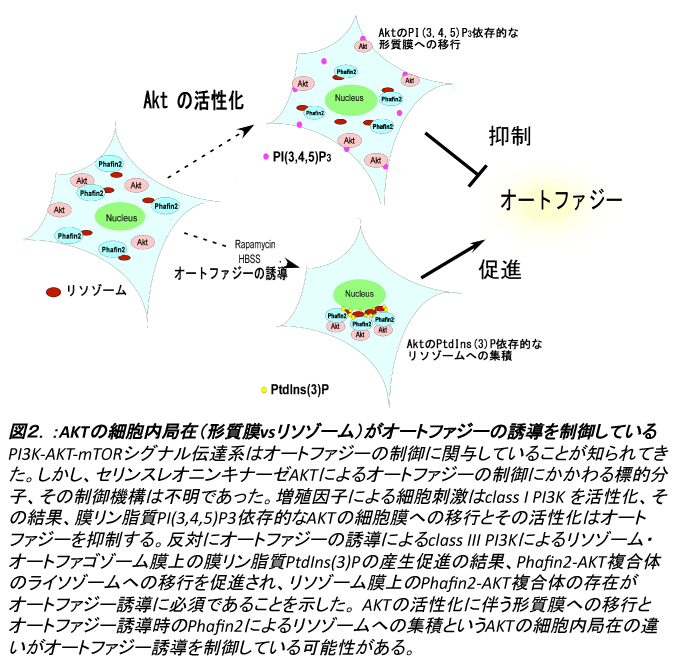
偙傟傑偱丄儕僜僜乕儉傪夘偟偨僆乕僩僼傽僕乕偵偼AKT僔僌僫儖偑娭梌偟偰偄傞偙偲偑悇應偝傟偰偒偨[4,5]丅憹怋場巕偺巋寖偼嵶朎撪偺class I PI3K 妶惈壔傪懀偟丄偦偺戙幱嶻暔偱偁傞枌儕儞帀幙PI乮3丆4丆5乯P3埶懚揑側AKT偺嵶朎枌傊偺堏峴偼僆乕僩僼傽僕乕傪梷惂偡傞偙偲偑抦傜傟偰偒偨丅偟偐偟丄峺曣偵偼偦偺幚幙揑側ortholog偺懚嵼偟側偄 AKT僔僌僫儖偵傛傞捈愙揑側僆乕僩僼傽僕乕偺惂屼偺昗揑暘巕丄偝傜偵偼偦偺暘巕儗儀儖偱偺惂屼婡峔偺徻嵶偼晄柧偱偁偭偨丅
尋媶惉壥
巹偨偪偼偙傟傑偱偵AKT偵寢崌AKT場巕偵傛傞嵶朎斀墳偺惂屼偺暘巕婡峔偺夝柧偵岦偗偨尋媶傪恑傔偰偒偨[6,7]丅偙偺曽岦惈偱偺尋媶傪捠偟偰巹偨偪偼丄yeast two hybrid 朄側傜傃偵柶塽嫟捑朄傪梡偄偰儔僀僜僝乕儉乮lysosome乯偵嬊嵼偡傞AKT偵寢崌偡傞怴偟偄嵶朎撪暘巕乮Phafin2乯傪摨掕偟偨丅Phafin2偼儕僜僜乕儉偵懚嵼偡傞嵶朎撪彫婍姱偺桝憲側偳偵偐偐傢傞偙偲偑悇應偝傟偨pleckstrin homology 乮PH乯domain 側傜傃偵FYVE 乮Fab1-YotB-Vac1p-EEA1乯domain偐傜側傞25KD偺彫偝偄暘巕偱偁傞丅変乆偼偙偺Phafin2 偑PI3K-AKT-mTOR僔僌僫儖偵傛傝僆乕僩僼傽僕乕傊偺曽岦惈寛掕偺尞傪埇傞暘巕偲偟偰拲栚偟丄偦偺夝愅傪恑傔偨丅Phafin2偼妶惈壔側傜傃偵旕妶惈壔AKT偲傕偵寢崌偡傞偙偲偑妋擣偱偒偨丅寀岝怓慺傪梡偄偨嫟徟揰尠旝嬀丄sucrose-gradient 朄偵傛傞儕僜僝乕儉偺惛惢丄暘巕僀儊乕僕儞僌乮FRET丄BiFC乯朄偵傛傝Phafin2乚AKT暋崌懱偺儕僜僝乕儉傊偺嬊嵼偲偦偺廤愊偑HBSS傗Rapamycin偵傛傞僆乕僩僼傽僕乕偺桿摫偵傛傝憹嫮偝傟傞偙偲傪帵偟偨丅Phafin2偼僆乕僩僼傽僕乕桿摫偵傛傝嵶朎幙偵懚嵼偡傞AKT偲寢崌偟丄Phafin2-AKT暋崌懱偲偟偰儕僜僝乕儉枌忋偺枌儕儞帀幙PtdIns(3)P埶懚揑偵儕僜僝乕儉偵堏峴偡傞丄偙偺僾儘僙僗偑僆乕僩僼傽僕乕偺桿摫偵偼嬌傔偰廳梫偱昁恵偱偁傞偙偲偑柧傜偐偲側偭偨丅僆乕僩僼傽僕乕桿摫偵偼Phafin2偲儕僜僝乕儉枌忬偵偁傞枌儕儞帀幙PtdIns(3)P偲偺寢崌偑昁恵偱偁傞偙偲丄偝傜偵僆乕僩僼傽僕乕桿摫側傜傃偵偦偺婡擻偵偼AKT側傜傃偵Phafin2偺懚嵼偑昁恵偱偁傞偙偲傪柧傜偐偵偟偨[8]丅
峫嶡
杮尋媶偱偼AKT偺怴婯寢崌場巕偲偟偰PH domain, FYVE domain偺擇偮偺枌儕儞帀幙PI(3)P寢崌僪儊僀儞傪帩偮儕僜僝乕儉僞儞僷僋Phafin2傪摨掕偟偨丅僆乕僩僼傽僕乕偺桿摫偵傛傝AKT偑儕僜僝乕儉偵懚嵼偡傞枌儕儞帀幙PtdIns(3)P埶懚揑偵Phafin2偵傛傝儕僜僝乕儉偵廤愊偡傞偙偲偑柧傜偐偲側偭偨丅偙偺Phafin2-AKT暋崌懱偺枌儕儞帀幙PtdIns(3)P埶懚揑側儕僜僝乕儉傊偺堏峴丄廤愊偑僆乕僩僼傽僕乕桿摫偵昁恵側process偱偁傞偙偲偑柧傜偐偵側偭偨丅崱夞偺尋媶惉壥偵傛傝Phafin2乚AKT暋崌懱偼偙傟傑偱峀偔梡偄傜傟偰偒偨僆乕僩僼傽僕乕慾奞嵻偱偁傞3-MA乮3-methyadenine乯[9]偺僆乕僩僼傽僕乕桿摫梷惂偵偐偐傢傞暘巕昗揑傪弶傔偰柧傜偐偵偡傞偙偲偑偱偒偨丅偙傟傑偱AKT偺妶惈壔偼僆乕僩僼傽僕乕桿摫傪梷惂揑偵嶌梡偡傞偙偲偑抦傜傟偰偒偨[5]丅偟偐偟丄崱夞偺尋媶偵傛傝AKT偺懚嵼帺懱丄偲偔偵AKT偺嵶朎撪偱偺暘晍偦偺傕偺偑僆乕僩僼傽僕乕偺桿摫偺寛掕偵嬌傔偰廳梫側偙偲偑柧傜偐偲側偭偨丅僆乕僩僼傽僕乕偺桿摫偵傛傝Phafin2偲偲傕偵堏峴丄儕僜僝乕儉偵廤愊偟偨AKT偑偳偺傛偆側摥偒傪偟偰偄傞偺偐偼崱屻偺尋媶偵傛傞夝柧偑懸偨傟傞丅僆乕僩僼傽僕乕偺惂屼偺棎傟偵傛傞僞儞僷僋幙暘夝宯偺堎忢偼丄惛恄恄宱幘姵傗埆惈庮釃丄姶愼徢側偳條乆側僸僩偺幘姵傪堷偒婲偙偡偙偲偑抦傜傟偰偄傞丅偟偐傞偵堦楢偺尋媶偼丄嵶朎撪PI3K- AKT-mTOR僔僌僫儖揱払偵傛傞僆乕僩僼傽僕乕惂屼偺巇慻傒偑柧傜偐偵偡傞偽偐傝偱側偔丄Phafin2- AKT暋崌懱傪夘偟偨僆乕僩僼傽僕乕傪惂屼偡傞偙偲偱敪偑傫丄僂僀儖僗姶愼丄Alzheimer昦側偳偵偍偗傞昦懺傗嵶朎斀墳偺惂屼偺奐敪偵岦偗偨摴昗偲側傞壜擻惈偑偁傞丅
嶲峫暥專
1. Noguchi M, Obata T, Suizu F (2008) Regulation of the PI3K-Akt Network: Current Status and a Promise for the Treatment of Human Diseases. Curr Sig Thera.
2. Noguchi M, Ropars V, Roumestand C, Suizu F (2007) Proto-oncogene TCL1: more than just a coactivator for Akt. FASEB J 21: 2273-2284.
3. Mizushima N, Levine B, Cuervo AM, Klionsky DJ (2008) Autophagy fights disease through cellular self-digestion. Nature 451: 1069-1075.
4. Lum JJ, DeBerardinis RJ, Thompson CB (2005) Autophagy in metazoans: cell survival in the land of plenty. Nat Rev Mol Cell Biol 6: 439-448.
5. Arico S, Petiot A, Bauvy C, Dubbelhuis PF, Meijer AJ, et al. (2001) The tumor suppressor PTEN positively regulates macroautophagy by inhibiting the phosphatidylinositol 3-kinase/protein kinase B pathway. Journal of Biological Chemistry 276: 35243-35246.
6. Laine J, Kunstle G, Obata T, Sha M, Noguchi M (2000) The protooncogene TCL1 is an Akt kinase coactivator. Mol Cell 6: 395-407.
7. Suizu F, Hiramuki Y, Okumura F, Matsuda M, Okumura AJ, et al. (2009) The E3 ligase TTC3 facilitates ubiquitination and degradation of phosphorylated Akt. Dev Cell 17: 800-810.
8. Matsuda-Lennikov M, Suizu F, Hirata N, Hashimoto M, Kimura K, et al. (2014) Lysosomal interaction of akt with phafin2: a critical step in the induction of autophagy. PLoS One 9: e79795.
9. Seglen PO, Gordon PB (1982) 3-Methyladenine: specific inhibitor of autophagic/lysosomal protein degradation in isolated rat hepatocytes. Proceedings of the National Academy of Sciences of the United States of America 79: 1889-1892.